Tiêu chuẩn quốc gia TCVN 10713-2:2015 (ISO 15788-2:2003) về Dầu mỡ động vật và thực vật - Xác định các stigmastadiene trong dầu thực vật - Phần 2: Phương pháp sắc kí lỏng hiệu năng cao (HPLC)
TIÊU CHUẨN QUỐC GIA
TCVN 10713-2:2015
ISO 15788-2:2003
DẦU MỠ ĐỘNG VẬT VÀ THỰC VẬT – XÁC ĐỊNH CÁC STIGMASTADIENE TRONG DẦU THỰC VẬT – PHẦN 2: PHƯƠNG PHÁP SẮC KÍ LỎNG HIỆU NĂNG CAO (HPLC)
Animal and vegetable fats and oils – Determination of stigmastadienes in vegetable oils – Part 2: Method using high-performance liquid chromatography (HPLC)
Lời nói đầu
TCVN 10713-2:2015 hoàn toàn tương đương với ISO 15788-2:2003;
TCVN 10713-2:2015 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F2 Dầu mỡ động vật và thực vật biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố;
Bộ tiêu chuẩn TCVN 10713 (ISO 15788) Dầu mỡ động vật và thực vật – Xác định các stigmastadiene trong dầu thực vật gồm có các phần sau:
- TCVN 10713-1:2015 (ISO 15788-1:1999), Phần 1: Phương pháp sắc kí khí cột mao quản (Phương pháp chuẩn);
- TCVN 17013-2:2015 (ISO 15788-2:2003), Phần 2: Phương pháp sắc kí lỏng hiệu năng cao (HPLC).
DẦU MỠ ĐỘNG VẬT VÀ THỰC VẬT – XÁC ĐỊNH CÁC STIGMASTADIENE TRONG DẦU THỰC VẬT – PHẦN 2: PHƯƠNG PHÁP SẮC KÍ LỎNG HIỆU NĂNG CAO (HPLC)
Animal and vegetable fats and oils – Determination of stigmastadienes in vegetable oils – Part 2: Method using high-performance liquid chromatography (HPLC)
1. Phạm vi áp dụng
Tiêu chuẩn này qui định phương pháp xác định các steradiene, đặc biệt là các stigmastadiene. Các steradiene được hình thành do sự mất nước của các sterol trong quá trình tẩy trắng, còn một phần được hình thành trong quá trình làm sạch bằng hơi nước và khử mùi. Phương pháp này cũng thích hợp làm phương pháp sàng lọc để phát hiện sự có mặt của dầu thực vật tinh luyện trong dầu nguyên chất như dầu ô liu nguyên chất.
CHÚ THÍCH TCVN 10713-1 (ISO 15788-1) là phương pháp chuẩn để xác định các stigmastadiene trong dầu thực vật, trong khi tiêu chuẩn này có thể được dùng như phương pháp sàng lọc nhanh. Trong độ chụm của phương pháp này (xem Phụ lục A), các mẫu dầu ô liu nguyên chất có chứa hàm lượng các chất này gần với giới hạn qui định quốc tế (IOOC, EC) có thể đánh giá xác nhận lại bằng phương pháp sắc kí khí lỏng (GLC) nêu trong TCVN 10713-1 (ISO 15788-1).
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851:1989, (ISO 3696:1987), Nước dùng để phân tích trong phòng thử nghiệm - Yêu cầu kỹ thuật và phương pháp thử
ISO 12228, Animal and vegetable fats and oils - Determination of individual and total sterols contents - Gas chromatographic method (Dầu mỡ động vật và thực vật – Xác định hàm lượng các sterol đơn lẻ và tổng số)
3. Thuật ngữ và định nghĩa
Trong tiêu chuẩn này, áp dụng các thuật ngữ và định nghĩa sau đây:
3.1. Hàm lượng các stigmastadiene (stigmastadienes content)
Phần các stigmastadiene tách được bằng sắc kí lỏng ở các điều kiện qui định trong tiêu chuẩn này.
CHÚ THÍCH Hàm lượng các stigmastadiene được tính bằng miligam trên kilôgam.
3.2. Hàm lượng các steradiene (steradienees content)
Phần của tất cả các steradiene tách được bằng sắc kí lỏng ở các điều kiện qui định trong tiêu chuẩn này.
CHÚ THÍCH Hàm lượng các steradiene được tính bằng miligam trên kilôgam.
4. Nguyên tắc
Các steradiene được tách ra khỏi phần chính của các lipid khác như các hợp chất béo không phân cực bằng ete dầu mỏ trên cột silica gel. Chất rửa giải ete dầu mỏ được cô đặc rồi được phân tích bằng sắc kí lỏng hiệu năng cao cột C18 pha đảo (RP-18 - HPLC) và detector UV ở bước sóng 235 nm. Sau đó chúng được định lượng, tùy thuộc vào loại mẫu, sử dụng chất chuẩn nội hoặc chuẩn ngoại.
5. Thuốc thử
CẢNH BÁO – Cần chú ý các qui định cụ thể về việc xử lý các chất gây nguy hiểm. Các tổ chức và cá nhân phải tuân thủ các biện pháp kỹ thuật an toàn.
Chỉ sử dụng các thuốc thử đạt chất lượng tinh khiết phân tích, trừ khi có các qui định khác.
5.1. Nước, ít nhất loại 1 của TCVN 4851:1989 (ISO 3696:1987).
5.2. Silica gel 60 dùng cho sắc kí cột, cỡ hạt từ 0,063 mm đến 0,200 mm hoặc từ 0,063 mm đến 0,100 mm1), có hàm lượng nước 2 g trên 100 g.
Sấy silica gel trong đĩa sứ 12 h ở 160 oC trong tủ sấy và để nguội trong bình hút ẩm đến nhiệt độ phòng. Để đưa silica gel đến hàm lượng nước 2 g/100 g, thì cân (chính xác đến 1 g) 98 g silica gel đã khô cho vào bình nón có nắp đậy thủy tinh mài rồi thêm 2 g nước (được cân chính xác đến 0,01 g). Lắc mạnh trong 1 min rồi để yên silica gel trong bình kín khí qua đêm.
5.3. Ete dầu mỏ, dải sôi từ 40 oC đến 60 oC.
5.4. Axetonitril, loại dùng cho sắc kí.
5.5. tert-Butyl metyl ete, loại dùng cho sắc kí.
5.6. Isooctan.
5.7. D3,5-Cholestadiene2), có độ tinh khiết đã biết ít nhất 95 g trên 100 g.
Kiểm tra độ tinh khiết của chất chuẩn cholestadiene bằng sắc kí khí, dùng 5a-cholestane làm chất chuẩn nội. Đối với phép thử này, xem các điều kiện về phương pháp sắc kí khí để xác định các sterol được qui định trong ISO 12228. Hệ số đáp ứng của detector ion hóa ngọn lửa phải là 1,0. Cần tính đến nồng độ thu được trong phép xác định các steradiene.
5.8. Dung dịch gốc và dung dịch chuẩn
5.8.1. Dung dịch gốc D3,5-cholestadiene, nồng độ 1 mg/ml.
Cân 50,0 mg D3,5-cholestadiene, chính xác đến 0,1 mg, cho vào bình định mức dung tích 50 ml. Hòa tan và pha loãng bằng tert-butyl metyl ete (5.5) đến vạch.
5.8.2. Dung dịch chuẩn D3,5-cholestadiene dùng cho HPLC
5.8.2.1. Dung dịch chuẩn ngoại, nồng độ 10 mg/ml.
Dùng pipet lấy 100 ml dung dịch gốc D3,5-cholestadiene (5.8.1) cho vào bình định mức 10 ml rồi đổ đầy axetonitril/tert-butyl metyl ete đến vạch (5.8.4).
20 ml dung dịch này chứa 0,20 mg cholestadiene. Dung dịch này được bơm lên cột HPLC. Nồng độ của dung dịch chuẩn phụ thuộc vào bản chất của loại dầu được phân tích. Trong trường hợp dầu nguyên chất có hàm lượng stigmastadiene nhỏ hơn 0,5 mg/kg, thì nồng độ của dung dịch chuẩn ngoại phải là 0,2 mg/ml.
5.8.2.2. Dung dịch chuẩn nội, nồng độ 2 mg/ml.
Dùng pipet lấy 100 ml dung dịch gốc m3,5-cholestadiene (5.8.1) cho vào bình định mức 50 ml và thêm ete dầu mỏ (5.3) đến vạch.
Nồng độ yêu cầu của dung dịch chuẩn phụ thuộc vào bản chất của dầu được phân tích. Trong trường hợp dầu nguyên chất có hàm ượng các stigmastadiene nhỏ hơn 0,5 mg/kg, thì nồng độ của dung dịch chuẩn nội phải là 0,2 mg/kg.
5.8.3. Dung dịch chuẩn 5a-cholestane dùng cho GC, nồng độ 1 mg/ml.
Cân 50,0 mg 5a-cholestadiene3), chính xác đến 0,1 mg, cho vào bình định mức dung tích 50 ml và thêm isooctan (5.6) đến vạch. Sử dụng dung dịch này để xác định độ tinh khiết của chuẩn D3,5-cholestadiene (5.8.2) như sau.
Dùng pipet lấy 1 ml mỗi dung dịch chuẩn 5a-cholestane3) và dung dịch gốc D3,5-cholestadiene (5.8.1) cho vào bình đong 10 ml (bơm chia dòng) hoặc cho vào bình định mức 50 ml (bơm lên cột) và thêm isooctan đến vạch.
5.8.4. Axetonitril/tert-butyl metyl ete, [50:50 (tính theo thể tích)].
5.8.5. Pha động dùng cho HPLC: axetonitril/tert-butyl metyl ete, [70:30 (tính theo thể tích)], đã khử khí.
5.9. Cholestane, có độ tinh khiết đã biết ít nhất 95 g/100 g.
6. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ của phòng thử nghiệm thông thường và cụ thể sau đây:
6.1. Bông côttông hoặc bông thủy tinh.
Bông côttông có thể được khử chất béo bằng cách chiết 8 h trong ete dầu mỏ.
6.2. Cột sắc kí, bằng thủy tinh, đường kính trong 10 mm, dài 150 mm, có bình chứa dung tích 25 ml.
6.3. Bình hình côn, dung tích 25 ml.
6.4. Bình định mức, dung tích 5 ml, 10 ml và 50 ml.
6.5. Cốc có mỏ, có nhiều cỡ.
6.6. Hệ thống HPLC, gồm có bơm, dụng cụ bơm mẫu (vòng bơm mẫu 20 ml và 100 ml), detector UV dùng để đo ở bước sóng 235 nm và hệ thống tích phân.
6.7. Cột HPLC, dài 250 mm, đường kính trong 4,0 mm hoặc 4,6 mm, có pha đảo kiểu RP 18 và cỡ hạt 5 mm 4).
6.8. Lọ lấy mẫu tự động, dung tích phù hợp.
6.9. Bộ cô quay, có nồi cách thủy.
7. Lấy mẫu
Mẫu gửi đến phòng thử nghiệm phải là mẫu đại diện. Mẫu không bị hư hỏng hoặc thay đổi trong suốt quá trình vận chuyển hoặc bảo quản.
Việc lấy mẫu không quy định trong tiêu chuẩn này. Nên lấy mẫu theo TCVN 2625 (ISO 5555).
8. Chuẩn bị mẫu thử
8.1. Yêu cầu chung
Loại bỏ nước ra khỏi mẫu chứa chất béo trước khi phân tích, nếu cần, bằng cách đun khoảng 5 g mẫu đến 100 oC trong khoảng thời gian ngắn rồi li tâm.
Nút đáy cột sắc ký bằng miếng bông (6.1) nhỏ.
Thêm 5 g silica gel (5.2) không có dung môi vào cột và nhồi cột bằng cách gõ nhẹ cột qua một miếng gỗ.
8.2. Phương pháp ngoại chuẩn
Cân khoảng 500 mg mẫu, chính xác đến 1 mg, cho vào cốc nhỏ có mỏ. Hòa tan mẫu trong 2 ml ete dầu mỏ và rót dung dịch này lên cột đã mở khóa. Tráng cốc có mỏ hai lần, mỗi lần 2 ml ete dầu mỏ.
Ngay khi dung môi chảy cạn đến đỉnh cột nhồi, rửa giải các chất không phân cực bằng 20 ml ete dầu mỏ rồi thu vào bình cầu (6.3).
Làm bay hơi dung môi đến khô trên bộ cô quay và hòa tan phần còn lại trong 500 ml axetonitril/tert-butyl metyl ete (5.8.4).
8.3. Phương pháp nội chuẩn
Khi dùng phương pháp này, đảm bảo rằng mẫu không còn chứa một lượng nhỏ D3,5-cholestadiene (ví dụ, dầu tinh luyện).
Cân khoảng 500 mg mẫu, chính xác đến 1 mg, cho vào cốc nhỏ có mỏ. Thêm 1,0 ml dung dịch chuẩn nội D3,5-cholestadiene. Hòa tan trong 2 ml ete dầu mỏ và rót dung dịch này lên cột đã mở khóa. Tráng cốc có mỏ hai lần, mỗi lần 2 ml ete dầu mỏ.
Ngay khi dung môi chảy cạn đến đỉnh cột nhồi, rửa giải các chất không phân cực bằng 20 ml ete dầu mỏ rồi thu vào bình hình côn (6.3).
Làm bay hơi dung môi đến khô trên bộ cô quay và hòa tan phần còn lại trong khoảng 500 ml axetonitril/tert-butyl metyl ete (5.8.4).
9. Cách tiến hành
9.1. Sắc kí lỏng hiệu năng cao (HPLC)
Các điều kiện sau đây có thể cho thấy thích hợp:
pha tĩnh: RP-18, cỡ hạt 5 mm;
kích thước cột: 250 mm x 4,6 mm;
pha động: axetonitril/tert-butyl metyl ete (5.8.5);
tốc độ dòng: 1 ml/min;
thể tích bơm: 20 ml đến 100 ml (tùy thuộc vào nồng độ dự kiến);
detector: UV, bước sóng 235 nm.
9.2. Nhận biết các steradiene
Nhận biết và khẳng định các pic bằng cách sử dụng thời gian lưu tương đối nêu trong Bảng 1 (xem thêm các sắc ký đồ trong Phụ lục B). Các cholestadiene cũng như chất đối chứng sẽ rửa giải sau từ 20 min đến 25 min.
Bảng 1 – Thời gian lưu tương đối của các dẫn xuất sterol
|
Dẫn xuất sterol |
Thời gian lưu tương đối (RRT) |
|
Cholestadiene |
1,00 |
|
Stigmastadien |
1,05 |
|
Campestadien |
1,07 |
|
Stigmastadien |
1,15 |
CHÚ THÍCH Tùy thuộc vào dầu hoặc chất béo được phân tích, mà dự kiến có các steradiene và các steratriene. Việc nhận biết các pic có thể thực hiện bằng cách bơm mẫu dầu tinh luyện hoặc chất béo hoặc bằng chính chất chuẩn stigmastadiene. Ở các điều kiện sắc kí đã cho, sắc ký đồ của dầu chưa qua xử lý (chưa tẩy trắng) không cho thấy có bất kỳ các pic nào trong phần sắc đồ có các steradiene sẽ được dự kiến.
10. Biểu thị kết quả
10.1. Chất chuẩn ngoại
Tính hàm lượng của các stigmastadiene hoặc steradiene, w, tính bằng miligam trên kilôgam, theo hàm lượng của cholestadiene trong chất chuẩn ngoại, như sau:
![]()
Trong đó
As là diện tích của pic stigmasta-3,5-diene hoặc diện tích của các pic steradiene;
M là khối lượng của cholesta-3,5-diene (chất chuẩn ngoại) (5.8.2.1) được bơm, tính bằng microgam (mg);
Ac là diện tích của pic cholesta-3,5-diene (chất chuẩn ngoại: nếu pic bị phân tách thì lấy tổng của các diện tích như trong Phụ lục B);
m là khối lượng dầu được lấy (8.2), tính bằng gam (g);
f là hệ số pha loãng (dùng cho thể tích mẫu 500 ml và thể tích bơm 20ml, f =25).
Độ tinh khiết của cholestadiene sử dụng phải được kiểm tra (xem 5.8.3) và phải đạt tối thiểu 95 %. Sau đó không cần hiệu chính. Nếu không, phải hiệu chính khối lượng. Sử dụng cùng một hệ số đáp ứng đối với cholestadiene và cholestane.
Báo cáo kết quả đến hai chữ số thập phân.
10.2. Chất chuẩn nội
Tính hàm lượng của các stigmastadiene hoặc steradiene, w’, biểu thị bằng miligam trên kilôgam, theo hàm lượng của cholestadiene trong chất chuẩn nội, như sau:
![]()
Trong đó
As’ là diện tích của pic stigmasta-3,5-dien hoặc diện tích của các pic steradiene;
M’ là khối lượng của cholesta-3,5-dien (chất chuẩn nội) được thêm vào (5.8.2.2), tính bằng microgam (mg);
Ac’ là diện tích của pic cholesta-3,5-dien (chất chuẩn nội; nếu pic bị phân tách thì lấy tổng của các diện tích nêu trong Phụ lục B);
m’ là khối lượng của dầu được lấy (8.3), tính bằng gam (g).
Độ tinh khiết của cholestadiene sử dụng phải được kiểm tra (xem 5.8.3) và phải đạt tối thiểu 95 %. Sau đó không cần hiệu chính. Nếu không, phải hiệu chính khối lượng. Sử dụng cùng một hệ số đáp ứng đối với cholestadiene và cholestane.
Báo cáo kết quả đến hai chữ số thập phân.
11. Độ chụm
11.1. Phép thử liên phòng thử nghiệm
Các chi tiết của phép thử liên phòng thử nghiệm về độ chụm được nêu trong Phụ lục A. Các giá trị thu được từ phép thử liên phòng thử nghiệm này có thể không áp dụng cho các dải nồng độ và các nền mẫu khác với các dải nồng độ và các nền mẫu đã nêu.
11.2. Độ lặp lại
Chênh lệch tuyệt đối giữa hai kết quả thử nghiệm độc lập, riêng rẽ, thu được khi sử dụng cùng một phương pháp thử, tiến hành trên cùng một vật liệu thử, thực hiện trong cùng một phòng thử nghiệm, do một người phân tích, sử dụng cùng thiết bị, trong một khoảng thời gian ngắn, không được quá 5 % các trường hợp vượt quá giá trị, r, nêu trong Bảng A.1, Phụ lục A.
11.3. Độ tái lập
Chênh lệch tuyệt đối giữa hai kết quả thử nghiệm riêng rẽ thu được thu được khi sử dụng cùng một phương pháp thử, tiến hành trên cùng một vật liệu thử, thực hiện trong các phòng thử nghiệm khác nhau, do những người khác nhau thực hiện, sử dụng các thiết bị khác nhau, vượt quá giới hạn tái lập, R, nêu trong Bảng A.1, Phụ lục A.
12. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải ít nhất bao gồm các thông tin sau đây:
a) mọi thông tin cần thiết về nhận biết đầy đủ về mẫu thử;
b) phương pháp lấy mẫu đã sử dụng, nếu biết;
c) phương pháp thử đã sử dụng, viện dẫn tiêu chuẩn này;
d) mọi chi tiết thao tác không quy định trong tiêu chuẩn này, hoặc được coi là tuỳ chọn, cùng với mọi tình huống bất thường có thể ảnh hưởng đến kết quả.
e) kết quả thử nghiệm thu được;
f) nếu đáp ứng yêu cầu về độ lặp lại thì nêu kết quả cuối cùng thu được.
Phụ lục A
(Tham khảo)
Các kết quả của phép thử liên phòng thử nghiệm
Độ chụm của phương pháp đã được thiết lập bởi phép thử liên phòng thử nghiệm quốc tế, tiến hành theo TCVN 6910-1 (ISO 5725-1) và TCVN 6910-2 (ISO 5725-2) do Đức tổ chức năm 1998, thử nghiệm trên năm mẫu khác nhau trong đó có 15 phòng thử nghiệm tham gia.
Bảng A.1 – Kết quả của phép thử liên phòng thử nghiệm
|
Mẫu |
Dầu ôliu nguyên chất |
Dầu ôliu nguyên chất có lượng dầu ôliu tinh luyện khác nhau |
|||
|
A |
B |
C |
D |
E |
|
|
Số lượng các phòng thử nghiệm tham gia |
15 |
15 |
15 |
15 |
15 |
|
Số lượng các phòng thử nghiệm được giữ lại sau khi trừ ngoại lệ |
12 |
15 |
14 |
15 |
15 |
|
Giá trị trung bình (mg/kg) |
0,01 |
0,11 |
0,18 |
0,32 |
0,15 |
|
Độ lệch chuẩn lặp lại (sr), mg/kg |
0,000 |
0,015 |
0,012 |
0,021 |
0,011 |
|
Độ lệch chuẩn tương đối lặp lại, % |
0 |
13 |
7 |
9 |
7 |
|
Giới hạn lặp lại (r) [sr x 2,8], mg/kg |
0,000 |
0,042 |
0,034 |
0,059 |
0,031 |
|
Độ lệch chuẩn tái lập (sR) mg/kg |
0,016 |
0,034 |
0,056 |
0,100 |
0,034 |
|
Độ lệch chuẩn tương đối tái lập, % |
144 |
30 |
31 |
31 |
23 |
|
Giới hạn tái lập (R) [sR x 2,8], mg/kg |
0,044 |
0,096 |
0,155 |
0,2794 |
0,095 |
Phụ lục B
(Tham khảo)
Các ví dụ về sắc ký đồ
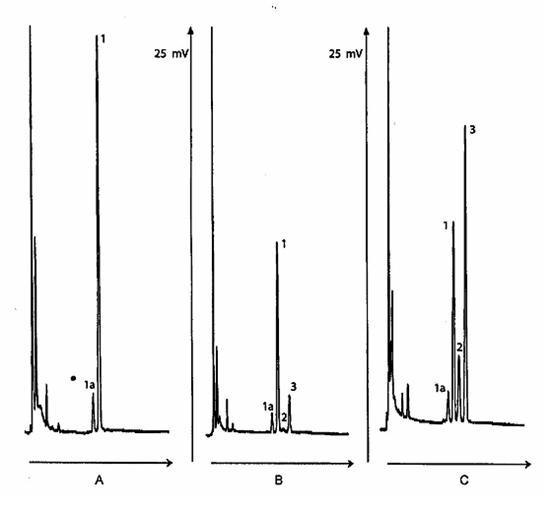
Nhận biết pic
Pic 1a/1 (17,5 min/20,3 min) cholestane
Pic 2 (21,8 min) campestadiene chính
Pic 3 (23,6 min) stigmastadiene
CHÚ THÍCH Một số cột không tách pic 1 a và 1.
Sắc ký đồ A: dầu ôliu nguyên chất đặc biệt, không phát hiện có các stigmastadiene
Sắc đồ B: dầu ô liu có các stigmastadiene hàm lượng 0,25 mg/kg
Sắc ký đồ C: dầu ôliu tinh luyện một phần có hàm lượng 2,5 mg/kg
Hình B.1
THƯ MỤC TÀI LIỆU THAM KHẢO
1] TCVN 2625:2007 (ISO 5555:2001), Dầu mỡ động vật và thực vật – Lấy mẫu
[2] TCVN 6910-1:2001 (ISO 5725-1:1994), Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo – Phần 1: Nguyên tắc và định nghĩa chung
[3] TCVN 6910-2:2001 (ISO 5725-2:1994), Độ chính xác (độ đúng và độ chụm) của phương pháp đo và kết quả đo – Phần 2: Phương pháp cơ bản xác định độ lặp lại và độ tái lập của phương pháp đo tiêu chuẩn
[4] SCHULTE E, Determination of edible dat refining by HPLC of 3,5-steradiene, Fat Sci, Techol., 96, 1994, pp. 124-128
[5] LINBURG. and COX R.H. Stigmasta-3,5,22-triene and di-stigamasteryl ete. Can. J. Chem., 35, 1957, pp. 1237-1238
1) Ví dụ, số 7734 hoặc 15101 từ E.Merck, 64271, Đức.
2) Ví dụ, số C6012 từ Sigma chemie GmbH, Grunwalder weg 30, 82041 Deisenhofen, Đức. Thông tin này đưa ra tạo thuận tiện cho người sử dụng tiêu chuẩn và không ấn định phải sử dụng sản phẩm này
3) Ví dụ, C8003 từ Sigma Chemie GmbH, Grunwalder weg 30, 82041 Deisengofen, Đức. Thông tin này đưa ra tạo thuận tiện cho người sử dụng tiêu chuẩn và không ấn định phải sử dụng sản phẩm này
4) Ví dụ, Supersphere 100, RP 18, Số 1.16858 từ E.Merck, 64271 Darmstadt, Đức. Thông tin này đưa ra tạo thuận tiện cho người sử dụng tiêu chuẩn và không ấn định phải sử dụng sản phẩm này.
