Tiêu chuẩn quốc gia TCVN 7102:2002 (CORESTA 38 : 1994) về Thuốc lá - Xác định đường khử bằng phương pháp phân tích dòng liên tục
TIÊU CHUẨN VIỆT NAM
TCVN 7102 : 2002
CORESTA 38 : 1994
THUỐC LÁ ĐIẾU - XÁC ĐỊNH ĐƯỜNG KHỬ BẰNG PHƯƠNG PHÁP PHÂN TÍCH DÒNG LIÊN TỤC
Tobacco - Determination of reducing carbohydrates by condinuous flow analysis
Lời nói đầu
TCVN 7102 : 2002 tương đương với CORESTA 38 : 1994 "Tobacco - Determination of reducing carbohydrates by continuous flow analysis" với các thay đổi biên tập cho phép.
TCVN 7102 : 2002 do Ban kỹ thuật tiêu chuẩn TCVN/TC 126 Thuốc lá và sản phẩm thuốc lá biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ ban hành.
THUỐC LÁ - XÁC ĐỊNH ĐƯỜNG KHỬ BẰNG PHƯƠNG PHÁP PHÂN TÍCH DÒNG LIÊN TỤC
Tobacco - Determination of reducing carbohydrates by condinuous flow analysis
1. Phạm vi áp dụng
Tiêu chuẩn này áp dụng cho thuốc lá đã chế biến và thuốc lá chưa chế biến.
2. Nguyên tắc
Chuẩn bị dịch chiết của thuốc lá bằng axit axetic 5 % (xem chú thích 1) và xác định hàm lượng đường khử trong dịch chiết bằng cách cho phản ứng với axit hidrazit p-hidroxibenzoic. Trong môi trường kiềm ở 85 oC, màu vàng osazon được tạo thành có độ hấp thụ cực đại ở bước sóng 410 nm.
Chú thích 1: Các nghiên cứu cộng tác cho thấy rằng đối với một số loại thuốc lá khi chiết bằng nước cất thì xảy ra sự thủy phân sucroza.
3. Thuốc thử
Tất cả các thuốc thử được sử dụng phải là loại tinh khiết phân tích và phù hợp với các qui định quốc gia hiện hành.
3.1. Dung dịch Brj 35 (ete lauryl polyoxietylen)
Cho 1 lít nước cất vào 250 g Brj 35, làm ấm và khuấy cho đến khi tan hết.
3.2. Dung dịch natri hidroxit (NaOH, 0,5 M)
Chuẩn bị 1 lít natri hidroxit 0,5 M từ các ampun hoặc hòa tan 20,0 g natri hydroxit trong 800 ml nước cất. Trộn và để nguội. Sau khi đã tan hết, cho thêm 0,5 ml dung dịch brj 35 (3.1) và pha loãng bằng nước cất đến 1 lít.
3.3. Dung dịch canxi clorua (CaCl2.6H2O, 0,008 M)
Hòa tan trong nước cất 1,75 g canxi clorua ngậm 6 phân tử nước (xem chú thích 2), thêm 0,5 ml dung dịch brij 35 (3.1) và pha loãng bằng nước cất đến 1 lít.
Chú thích: Nếu xẩy ra kết tủa thì lọc dung dịch qua giấy lọc Whatman số 1 (hoặc loại tương đương).
3.4. Dung dịch axit axetic, (CH3COOH, 5 % V/V)
Chuẩn bị dung dịch axit axetic 5 % (V/v) từ axit axetic "băng" (được sử dụng để chuẩn bị các chuẩn, các mẫu và để rửa dung dịch trên máy phân tích dòng liên tục).
3.5. Dung dịch axit clohidric (HCl, 0,5 M)
Cho 500 ml nước cất vào bình định mức 1 lít. Thêm từ từ 42 ml axit clohidric (37 % m/m). Pha loãng bằng nước cất đến vạch mức.
3.6. Dung dịch axit hydrazit p-hidrobenzoic (PAHBAH), (HOC6H4CONHNH2)
Cho 250 ml axit clohidric 0,5 M (3.5) vào bình định mức 500 ml. Thêm 25 g axit hidrazit p-hidrobenzoic và để cho tan hết. Thêm 10,5 g axit xitric ngậm 1 phân tử nước [HOC(CH2COOH)2COOH.H2O]. Pha loãng bằng dung dịch axit clohidric 0,5 M đến vạch mức. Bảo quản ở 5 oC và chỉ lấy một lượng vừa đủ ra khỏi tủ lạnh để dùng trong ngày.
Chú thích 3 - Độ tinh khiết của PAHBAH (> 97 % m/m) là rất quan trọng vì có thể tạo chất kết tủa trong dòng phân tích nếu có lẫn tạp chất. PAHBAH có thể kết tinh lại do nước cất (xem Beilstein 10,174). PAHBAH không tinh khiết khi thấy các có biểu hiện sau:
a) các hạt đen lẫn trong tinh thể PAHBAH màu trắng;
b) màu vàng trong dung dịch PAHBAH 5 % được pha chế trong axit clohidric 0,5 M;
c) khó hòa tan các tinh thể PAHBAH trong dung dịch natri hidroxit 0,5 M;
d) các hạt lạ nổi lên trong thuốc thử;
e) đường nền của thuốc thử có gợn sóng.
Dung dịch PAHBAH có thể được chuẩn bị như sau: Cho 250 ml dung dịch axit clohidric 0,5 M vào cốc, làm ấm đến 45 oC và vừa thêm PAHBAH vừa khuấy đều và cho axit xitric ngậm 1 phân tử nước vào dung dịch axit clohidric. Để nguội dung dịch, rồi chuyển sang bình định mức và pha loãng đến vạch. Thực tế cho thấy việc chuẩn bị dung dịch PAHBAH theo qui trình này tránh được sự hình thành kết tủa trong dòng phân tích.
3.7. D-glucoza (C6H12O6, loại tinh khiết phân tích) để chuẩn bị các chuẩn
Bảo quản trong bình hút ẩm.
3.8. Dung dịch glucoza tiêu chuẩn
3.8.1. Dung dịch gốc: Cân khoảng 10,0 g glucoza (3.7) chính xác đến 0,0001 g, hòa tan trong 800 ml axit axetic 5 % (3.4) và pha loãng bằng axit axetic (3.4) đến 1 lít trong bình định mức. Dung dịch này chứa khoảng 10 mg glucoza/ml. Bảo quản trong tủ lạnh. Hàng tháng chuẩn bị dung dịch mới.
3.8.2. Chuẩn làm việc: Từ dung dịch gốc tạo ra một loạt gồm ít nhất năm dung dịch hiệu chuẩn (trong 5 % axit axetic) chứa các nồng độ bao trùm dải nồng độ dự tính trong mẫu, thí dụ từ 0,2 mg glucoza/ml đến 1,8 mg glucoza/ml. Tính nồng độ chính xác của từng chất chuẩn. Bảo quản trong tủ lạnh. Cứ hai tuần thì chuẩn bị các dung dịch mới.
4. Thiết bị, dụng cụ
4.1. Các dụng cụ, thiết bị phòng thí nghiệm thông thường cần thiết cho việc chuẩn bị mẫu, các chuẩn và thuốc thử.
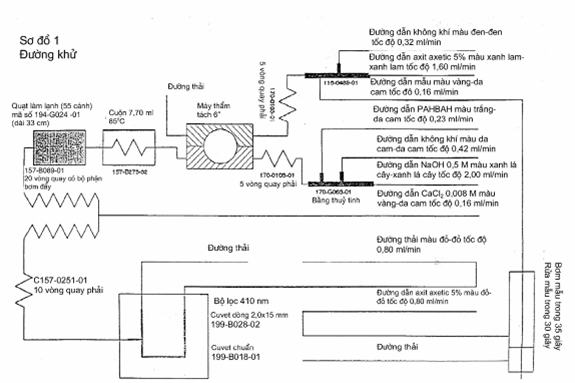
4.2. Máy phân tích dòng liên tục (xem sơ đồ 1) bao gồm:
- Bộ phận lấy mẫu;
- Bơm định lượng;
- Máy thẩm tách;
- Bể gia nhiệt;
- Ống xoắn làm chậm;
- Máy so màu (hoặc máy tương đương) được trang bị các bộ lọc ở bước sóng 410 nm;
Máy ghi.
5. Phân tích mẫu thuốc lá
5.1. Chuẩn bị mẫu thuốc lá để phân tích bằng cách nghiền (tất cả mẫu phải lọt qua sàng kích thước 1 mm) và xác định độ ẩm. Nếu thuốc lá quá ẩm thì trước khi nghiền nên sấy khô ở nhiệt độ không quá 40 oC.
5.2. Cân khoảng 250 mg thuốc lá chính xác đến 0,0001 g cho vào bình nón khô, dung tích 50 ml. Cho thêm 25 ml dung dịch axit axetic 5 % (3.4), đậy nắp bình và lắc trong 30 phút.
5.3. Lọc phần chiết qua giấy lọc Whatman số 40 (hoặc loại tương đương), loại bỏ một vài mililit đầu tiên của dịch, sau đó thu dịch lọc vào cốc phân tích.
5.4. Cho chạy các mẫu và các chất chuẩn qua hệ thống theo cách thông thường (nghĩa là: cho chạy 6 dịch chiết của thuốc lá, các chất chuẩn hiệu chuẩn và các mẫu, cứ sau 6 mẫu chạy xen kẽ 1 dung dịch hiệu chuẩn). Nếu các nồng độ của mẫu nằm ngoài dải nồng độ của các chuẩn thì phải pha loãng các mẫu và cho chạy lại.
6. Tính toán
6.1. Dựng đồ thị chiều cao pic theo các nồng độ nitrat tương ứng với tất cả các dung dịch hiệu chuẩn.
6.2. Tính phần trăm hàm lượng đường khử (tính theo khối lượng chất khô) trong thuốc lá theo công thức sau:
% đường khử (chất
khô)
= ![]()
trong đó
c là nồng độ đường khử thu được từ đường chuẩn (6.1), tính theo miligam trên mililit;
V là thể tích của dịch chiết đã chuẩn bị (5.2) (thường là 25 ml), tính bằng mililit;
m là khối lượng của mẫu (5.2), tính bằng miligam;
M là độ ẩm của thuốc lá (5.1), tính bằng phần trăm khối lượng.
Kết quả thử được tính đến một chữ số sau dấu phẩy.
Chú thích 4: Nếu phương pháp này được thực hiện đồng thời với phương pháp CORESTA 35 hoặc TCVN 7101 : 2002 (CORESTA 36) thì có thể chuẩn bị các chuẩn kết hợp.
7. Độ lặp lại và độ tái lập
Một nghiên cứu cộng tác quốc tế đã được tiến hành trong năm 1993 gồm 13 phòng thử nghiệm tham gia thực hiện trên 3 mẫu cho thấy rằng khi các cấp thuốc lá đơn được phân tích bằng phương pháp này thì thu được các giá trị độ lặp lại (r) và độ tái lập (R) sau đây.
Chênh lệch giữa hai kết quả đơn tìm thấy trên các dịch chiết khác nhau, do cùng một người thực hiện, sử dụng cùng thiết bị trong khoảng thời gian ngắn (thời gian phân tích 40 cốc mẫu) và nếu không hiệu chuẩn lại thiết bị trong suốt quá trình phân tích, thì kết quả sẽ vượt quá giá trị độ lặp lại (r) trung bình không quá một lần trong 20 trường hợp thao tác bình thường và đúng phương pháp.
Các kết quả đơn do hai phòng thử nghiệm thực hiện, chênh lệch quá giá trị tái lập (R) trung bình không quá một trong 20 trường hợp thao tác bình thường và đúng phương pháp.
Các số liệu phân tích cho đánh giá như tổng kết trong bảng 1.
Bảng 1
|
Loại thuốc lá |
Hàm lượng đường khử trung bình % (chất khô) |
Độ lặp lại r |
Độ tái lập R |
|
Burley |
0,6 |
0,4 |
0,6 |
|
Oriental |
14,5 |
1,6 |
3,3 |
|
Vàng sấy |
20,0 |
1,0 |
4,7 |
Để tính giá trị r và R, một kết quả thử nghiệm được coi là kết quả của một lần xác định đơn.
Phụ lục A
(Tham khảo)
Để tránh kết tủa PAHBAH, sử dụng ống tiêm có đường kính trong rộng (2 mm) để đưa dung dịch PAHBAH vào dòng phân tích. Ngoài ra, nồng độ của PAHBAH có thể bị giảm khi biết chắc rằng nồng độ PAHBAH sẽ vượt quá trong dòng phân tích. Điều này cũng hạn chế được kết tủa.
Tốt nhất là nên sử dụng cách trộn trực tiếp PAHBAH/NaOH (xem sơ đồ 1). Tuy nhiên, nếu kết tủa hình thành trực tiếp thì có thể trộn trước các dung dịch PAHBAH/NaOH hàng ngày và đưa thuốc thử hỗn hợp vào dòng phân tích. Thực nghiệm cho thấy rằng các kết quả tương tự thu được với điều kiện là thuốc thử hỗn hợp không được lưu giữ quá 8 giờ. Nếu sử dụng thuốc thử hỗn hợp thì có thể cần hiệu chỉnh đường nền do tín hiệu đường nền tăng.