Tiêu chuẩn quốc gia TCVN 8139:2009 (ISO 5554 : 1978) về Sản phẩm thịt - Xác định hàm lượng tinh bột (Phương pháp chuẩn)
TIÊU CHUẨN QUỐC GIA
TCVN 8139 : 2009
ISO 5554 : 1978
SẢN PHẨM THỊT - XÁC ĐỊNH HÀM LƯỢNG TINH BỘT (PHƯƠNG PHÁP CHUẨN)
Meat products - Determination of starch content (Reference method)
Lời nói đầu
TCVN 8139 : 2009 hoàn toàn tương đương với ISO 5554 : 1978;
TCVN 8139 : 2009 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F8 Thịt và sản phẩm thịt biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng đề nghị, Bộ Khoa học và Công nghệ công bố.
SẢN PHẨM THỊT - XÁC ĐỊNH HÀM LƯỢNG TINH BỘT (PHƯƠNG PHÁP CHUẨN)
Meat products - Determination of starch content (Reference method)
1. Phạm vi áp dụng
Tiêu chuẩn này qui định phương pháp chuẩn để xác định hàm lượng tinh bột trong sản phẩm thịt.
2. Lĩnh vực áp dụng
Tiêu chuẩn này chỉ áp dụng cho các sản phẩm không chứa các chất bổ sung không phải là tinh bột sinh ra đường khử khi thủy phân.
3. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
ISO 3100, Thịt và sản phẩm thịt - Lấy mẫu 1) .
4. Thuật ngữ, định nghĩa
Trong tiêu chuẩn này sử dụng thuật ngữ và định nghĩa sau đây:
Hàm lượng tinh bột trong sản phẩm thịt (starch content of meat products):
Hàm lượng tinh bột xác định được theo qui trình qui định trong tiêu chuẩn này và được biểu thị theo phần trăm khối lượng.
5. Nguyên tắc
Đun nóng phần mẫu thử với dung dịch kali hydroxit trong etanol cho đến khi các thành phần thịt hòa tan hết. Gạn, rửa cặn còn lại bằng etanol nóng, lọc, hòa tan trong axit clohydric và thủy phân. Xác định bằng chuẩn độ glucoza tạo thành.
6. Thuốc thử
Chỉ sử dụng các thuốc thử đạt chất lượng tinh khiết phân tích. Nước được sử dụng phải là nước cất hoặc ít nhất là nước có độ tinh khiết tương đương.
6.1 Kali hydroxit, dung dịch trong etanol.
Hòa tan 50 g kali hydroxit trong 800 ml etanol 95 % (thể tích) và pha loãng bằng etanol đến 1000 ml.
6.2 Etanol, 80% (thể tích).
6.3 Axit clohydric, dung dịch 1,0 M (không chứa clorua).
6.4 Xanh bromotymol, dung dịch 10 g/l trong etanol 95% (thể tích).
6.5 Natri hydroxit, dung dịch 300 g/l.
6.6 Dung dịch làm kết tủa protein
Dung dịch I
Hòa tan trong nước 106 g kali hecxaxyanoferat (II) ngậm ba phân tử nước [K4Fe(CN)6.3H2O] đựng trong bình định mức một vạch 1 000 ml và pha loãng đến vạch.
Dung dịch II
Hòa tan 220 g kẽm axetat ngậm hai phân tử nước [Zn(CH3COO)2.2H2O] trong nước đựng trong bình định mức một vạch 1 000 ml. Thêm 30 ml axit axetic băng và pha loãng bằng nước đến vạch.
6.7 Thuốc thử đồng
Chuẩn bị các dung dịch sau đây:
a) 25 g đồng (II) sulphat ngậm năm phân tử nước (CuSO4.5H2O) trong 100 ml nước;
b) 144 g natri cacbonat (Na2CO3) trong 300 ml đến 400 ml nước ở 50oC;
c) 50 g axit xitric ngậm một phân tử nước (C6H8O7.H2O) trong 50 ml nước.
Thêm từ từ và cẩn thận dung dịch c) vào dung dịch b) trong khi vẫn khuấy. Tiếp tục cho đến khi ngừng bay hơi cacbon dioxit.
Thêm dung dịch a) vào hỗn hợp này trong khi vẫn khuấy.
Để nguội đến nhiệt độ phòng, chuyển hết sang bình định mức một vạch 1 000 ml, pha loãng đến vạch và lọc sau 24h.
Hỗn hợp sau khi pha loãng 1 phần dung dịch này với 49 phần nước mới đun sôi và để nguội, phải có pH 10,0 ± 0,1.
6.8 Dung dịch chỉ thị tinh bột.
Cho hỗn hợp của 10 g tinh bột hòa tan, 10 mg thủy ngân (II) iođua (làm chất bảo quản) và 30 ml nước vào 1 lít nước sôi. Tiếp tục đun sôi trong 3 min và để nguội.
6.9 Natri thiosulfat, dung dịch chuẩn khoảng 0,1 N.
6.9.1 Chuẩn bị
Hòa tan 25 g natri thiosulfat ngậm năm phân tử nước (Na2S2O3.5H2O) trong 1000 ml nước vừa mới đun sôi, để nguội và thêm 0,2 g natri cacbonat ngậm mười phân tử nước (Na2CO3.10H2O). Để yên dung dịch một ngày trước khi chuẩn hóa.
6.9.1 Chuẩn hóa
Cân 150,0 mg kali iođat khô, hòa tan trong 25 ml nước và thêm 2 g kali iođua, 10 ml dung dịch axit clohydric (6.3).
Chuẩn độ bằng dung dịch thiosulfat trong khi khuấy liên tục. Thêm 1 ml dung dịch chỉ thị tinh bột (6.8) khi dung dịch có màu vàng nhạt và tiếp tục chuẩn độ cho đến khi mất màu xanh. Nồng độ đương lượng T của dung dịch natri thiosulfat tính được từ công thức:
![]()
trong đó
m là khối lượng của kali iođat, tính bằng miligam (mg);
V là thể tích của dung dịch natri thiosulfat đã bổ sung vào dung dịch kali iođat, tính bằng mililit (ml);
![]() phân
tử lượng tương đối của kali iođat.
phân
tử lượng tương đối của kali iođat.
6.10 Kali iođua, dung dịch 100 g/l.
Hòa tan 10 g kali iođua trong nước và thêm nước đến 100 ml. Bảo quản dung dịch trong lọ thủy tinh màu nâu sẫm.
6.11 Axit clohydric, dung dịch 25% (khối lượng)(không chứa clo).
Pha loãng 100 ml axit clohydric đậm đặc không chứa clo (r20 1,19 g/ml) bằng 60 ml nước.
7. Thiết bị, dụng cụ
Sử dụng các thiết bị, dụng cụ của phòng thử nghiệm thông thường, trừ khi có quy định khác và cụ thể như sau:
7.1 Máy xay thịt bằng cơ, cỡ phòng thử nghiệm, có gắn tấm đục lỗ, đường kính lỗ không quá 4 mm
7.2 Nồi cách thủy.
7.3 Giấy lọc gấp nếp, đường kính 15 cm, không chứa tinh bột.
7.4 Tấm amiăng, có lỗ tròn, gần với đáy bình món (7.5).
7.5 Bình nón, dung tích 250 ml đến 300 ml, có cổ mài và có nắp đậy bằng thủy tinh
7.6 Bình ngưng, làm lạnh bằng không khí, có khớp nối hình côn gắn với bình nón (7.5).
7.7 Hạt trợ sôi (ví dụ viên đá bọt hoặc bi thủy tinh).
7.8 Buret, dung tích 50 ml, phù hợp với loại A của TCVN 7149 : 2007 (ISO 385 : 2005).
7.9 Máy đo pH.
8. Lấy mẫu
8.1 Lấy ít nhất 200 g mẫu đại diện. Xem ISO 3100.
8.2 Bảo quản mẫu, nếu cần, sao cho không bị giảm chất lượng và thay đổi thành phần.
9. Cách tiến hành
9.1 Chuẩn bị mẫu thử
Dùng máy xay thịt (7.1) xay mẫu ít nhất hai lần và trộn đều để thu được mẫu đồng nhất. Bảo quản mẫu đã đồng nhất trong vật chứa kín khí, đậy nắp vật chứa và bảo quản sao cho không bị giảm chất lượng và thay đổi thành phần của mẫu. Phân tích mẫu càng sớm càng tốt, chỉ trong vòng 24 h sau khi đồng hóa.
9.2 Phần mẫu thử
Cân khoảng 25 g mẫu thử (9.1), chính xác đến 0,1 g, cho vào cốc có mỏ 500 ml hoặc 600 ml. Nếu khối lượng tinh bột trong phần mẫu thử dự đoán lớn hơn 1g, thì giảm khối lượng phần mẫu thử cho phù hợp.
9.3 Tách tinh bột
Cho 300 ml dung dịch kali hydroxit trong etanol nóng (6.1) vào phần mẫu thử trong khi liên tục khuấy bằng đũa thủy tinh và đậy cốc có mỏ bằng mặt kính đồng hồ. Đun trên nồi cách thủy (7.2) trong 1h, thỉnh thoảng khuấy. Gạn dung dịch qua giấy lọc (7.3) và dùng etanol nóng (6.2) rửa lượng tinh bột trên giấy lọc với sự hỗ trợ của đũa thủy tinh có đầu được bọc cao su. Giữ giấy lọc ướt.
CHÚ THÍCH Trong một số trường hợp, cho ly tâm tốt hơn lọc.
9.4 Thủy phân
Dùng đũa thủy tinh để tách chất kết tủa trên giấy lọc. Khoét một lỗ trên giấy lọc và rửa tinh bột qua lỗ bằng 100 ml dung dịch axit clohydric nóng (6.3) cho vào cốc có mỏ 250 ml. Đậy cốc có mỏ bằng mặt kính đồng hồ và ngâm cốc vào nồi cách thủy đang sôi trong 2,5h, thỉnh thoảng dùng đũa thủy tinh để khuấy dung dịch.
Làm nguội dung dịch và trung hòa bằng cách nhỏ từng giọt dung dịch natri hydroxit (6.5), tiến hành cẩn thận sao cho pH không quá 6,5; kiểm tra độ pH bằng máy đo pH (7.9).
Chuyển hết hỗn hợp vào bình định mức 200 ml, rửa bằng nước, thêm 3 ml Dung dịch I (6.6) và sau khi trộn đều thêm 3 ml Dung dịch II (6.6), pha loãng đến vạch.
Trộn đều và lọc qua giấy lọc gấp nếp (7.3). Ngay trước khi dùng pipet lấy phần dịch lỏng sử dụng cho giai đoạn tiếp theo, kiềm hóa dịch lọc làm chuyển sang xanh bromotylmol (6.4) bằng cách thêm 1 hoặc 2 giọt dung dịch natri hydroxit (6.5)
9.5 Xác định glucoza
Nếu chưa biết hàm lượng tinh bột xấp xỉ của mẫu, thì tiến hành phân tích sơ bộ để ước tính.
Pha loãng phần dịch lỏng (V2) của dịch lọc (9.4) bằng nước đến thể tích đã biết (V3) sao cho cứ 25 ml dung dịch pha loãng chứa từ 40 mg đến 50 mg glucoza và không có trường hợp nào quá 60 mg glucoza.
Trộn đều và dùng pipet lấy 25,0 ml dịch pha loãng cho vào bình nón (7.5). Dùng pipet lấy 25,0 ml thuốc thử đồng (6.7) cho vào bình và thêm một vài hạt trợ sôi (7.7).
CHÚ THÍCH Về cơ bản, tổng thể tích của dịch lỏng ở giai đoạn này là 50,0 ml.
Lắp bình ngưng (7.6) vào bình. Cho bình cầu và bình ngưng lên lưới kim loại được phủ tấm amiăng (7.4).
Đun dịch lỏng đến sôi trên bếp ga trong khoảng 2 min và tiếp tục đun sôi nhẹ trong đúng 10 min. Sau đó làm nguội nhanh đến nhiệt độ phòng. Lấy bình ngưng ra và thêm 30 ml dung dịch kali iođua (6.10) và thêm tiếp càng nhanh càng tốt 25 ml dung dịch axit clohydric (6.11). Đậy bình cho đến khi tiến hành chuẩn độ.
Chuẩn độ iot đã giải phóng bằng dung dịch natri thiosulfat chuẩn (6.9). Khi dung dịch có màu vàng nhạt, thì thêm khoảng 1 ml dung dịch chỉ thị tinh bột (6.8) và tiếp tục chuẩn độ cho đến khi màu xanh biến mất.
9.6 Xác định mẫu trắng
Tiến hành xác định mẫu trắng theo cùng một quy trình như trong 9.5, dùng 25,0 ml nước thay cho 25,0 ml dịch lọc pha loãng.
10. Biểu thị kết quả
10.1 Tính toán và công thức
Tính chênh lệch giữa các thể tích ghi lại được trong hai lần chuẩn độ, biểu thị bằng mililit dung dịch natri thiosulfat chính xác đến 0,1 N, theo công thức:
10 T x (Vo - V1)
trong đó
T là nồng độ đương lượng dung dịch natri thiosulfat chuẩn (xem 6.9.2);
Vo là thể tích dung dịch natri thiosulfat chuẩn (6.9) cần cho phép xác định mẫu trắng (9.6), tính bằng mililit (ml);
V1 là thể tích dung dịch natri thiosulfat chuẩn (6.9) cần cho dịch pha loãng (9.5), tính bằng mililit (ml).
Tính hàm lượng tinh bột, biểu thị bằng phần trăm khối lượng, theo công thức:
![]()
trong đó
V2 là thể tích phần dịch lọc chưa pha loãng (xem 9.5), tính bằng mililit (ml);
V3 là thể tích phần dịch lọc pha loãng (xem 9.5), tính bằng mililit (ml);
mo là khối lượng phần mẫu thử (9.2), tính bằng gam (g);
m1 là khối lượng của glucoza được xác định được từ công thức 10 T x (Vo - V1) bằng cách đối chiếu trong Bảng 1 hoặc Hình 1, tính bằng miligam (mg);
0,9 là hệ số chuyển đổi khối lượng glucoza m1 tương ứng với khối lượng tinh bột.
Lấy kết quả chính xác đến 0,1 %.
10.2 Độ chụm
10.2.1 Độ lặp lại
Chênh lệch giữa các kết quả của hai lần xác định tiến hành đồng thời hoặc liên tục nhanh do cùng một người phân tích không vượt quá 0,2g tinh bột trên 100 g mẫu.
10.2.2 Độ tái lập
Chênh lệch giữa các kết quả của hai lần xác định tiến hành trong hai phòng thử nghiệm trên cùng mẫu thử không được vượt quá 0,3 g tinh bột trong 100 g mẫu.
11. Báo cáo thử nghiệm
Báo cáo thử nghiệm cần chỉ rõ phương pháp đã sử dụng và kết quả thu được. Báo cáo thử nghiệm cũng cần đề cập đến mọi chi tiết thao tác không được quy định trong tiêu chuẩn này, hoặc được xem là tùy ý, cùng với mọi tình huống bất thường có thể ảnh hưởng đến kết quả;
Báo cáo thử nghiệm cũng phải bao gồm mọi thông tin cần thiết để nhận biết đầy đủ về mẫu.
Phụ lục A
(Qui định)
Bảng 1 - Chuyển đổi mililit dung dịch natri thiosulfat 0,1 N sang miligam glucoza
|
10 T x (Vo - V1) |
Khối lượng glucoza tương ứng |
|
|
Số mililit dung dịch natri thiosulfat 0,1 N |
m1 mg |
Dm1 mg |
|
1 |
2,4 |
2,4 |
|
2 |
4,8 |
2,4 |
|
3 |
7,2 |
2,5 |
|
4 |
9,7 |
2,5 |
|
5 |
12,2 |
2,5 |
|
6 |
14,7 |
2,5 |
|
7 |
17,2 |
2,6 |
|
8 |
19,8 |
2,6 |
|
9 |
22,4 |
2,6 |
|
10 |
25,0 |
2,6 |
|
11 |
27,6 |
2,7 |
|
12 |
30,3 |
2,7 |
|
13 |
33,0 |
2,7 |
|
14 |
35,7 |
2,8 |
|
15 |
38,5 |
2,8 |
|
16 |
41,3 |
2,9 |
|
17 |
44,2 |
2,9 |
|
18 |
47,1 |
2,9 |
|
19 |
50,0 |
3,0 |
|
20 |
53,0 |
3,0 |
|
21 |
56,0 |
3,1 |
|
22 |
59,1 |
3,1 |
|
23 |
62,2 |
|
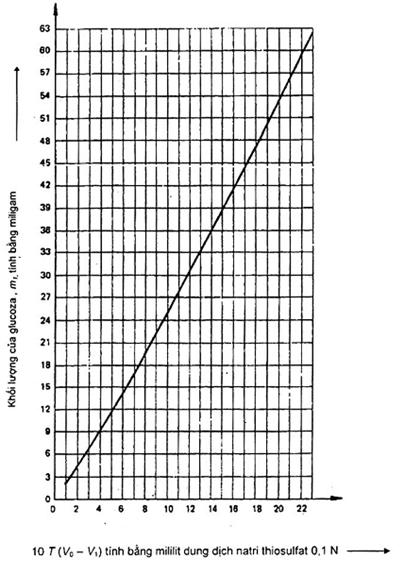
Hình 1 - Sơ đồ chuyển đổi mililit dung dịch natri thiosulfat 0,1 N sang miligam glucoza
1) ISO 3100 đã được thay thế bằng hai tiêu chuẩn ISO 3100-1 : 1991 (đã được biên soạn thành TCVN 4833-1 : 2002) và ISO 3100-2 : 1991 (đã được biên soạn thành TCVN 4833-2 : 2002).
Hiện nay, ISO 3100-1 : 1991 đã bị hủy và được thay thế bằng ISO 17604 : 2003 (được biên soạn thành TCVN 7925 : 2008 Vi sinh vật thực phẩm và thức ăn chăn nuôi - Phương pháp lấy mẫu thân thịt tươi để phân tích vi sinh vật).
