Tiêu chuẩn quốc gia TCVN 8905:2011 (EN 12632:1999) về Nước rau quả - Xác định hàm lượng axit axetic (Axetat) bằng enzym - Phương pháp đo phổ NAD
TIÊU CHUẨN QUỐC GIA
TCVN 8905:2011
EN 12632:1999
NƯỚC RAU QUẢ – XÁC ĐỊNH HÀM LƯỢNG AXIT AXETIC (AXETAT) BẰNG ENZYM – PHƯƠNG PHÁP ĐO PHỔ NAD
Fruit and vegetable juices – Enzymatic determination of acetic acid (acetate) content – NAD spectrometric method
Lời nói đầu
TCVN 8905:2011 hoàn toàn tương đương với EN 12632:1999;
TCVN 8905:2011 do Ban kỹ thuật tiêu chuẩn quốc gia TCVN/TC/F10 Rau quả và sản phẩm rau quả biên soạn, Tổng cục Tiêu chuẩn Đo lường Chất lượng thẩm định, Bộ Khoa học và Công nghệ công bố.
NƯỚC RAU QUẢ – XÁC ĐỊNH HÀM LƯỢNG AXIT AXETIC (AXETAT) BẰNG ENZYM – PHƯƠNG PHÁP ĐO PHỔ NAD
Fruit and vegetable juices – Enzymatic determination of acetic acid (acetate) content – NAD spectrometric method
1. Phạm vi áp dụng
Tiêu chuẩn này quy định phương pháp enzym để xác định hàm lượng tổng số của axit axetic cùng các muối axetat trong nước rau quả và các sản phẩm có liên quan.
2. Tài liệu viện dẫn
Các tài liệu viện dẫn sau rất cần thiết cho việc áp dụng tiêu chuẩn này. Đối với các tài liệu viện dẫn ghi năm công bố thì áp dụng phiên bản được nêu. Đối với các tài liệu viện dẫn không ghi năm công bố thì áp dụng phiên bản mới nhất, bao gồm cả các sửa đổi, bổ sung (nếu có).
TCVN 4851:1989 (ISO 3696:1987), Nước dùng để phân tích trong phòng thí nghiệm – Yêu cầu kĩ thuật và phương pháp thử.
3. Kí hiệu và chữ viết tắt
3.1. Kí hiệu
Trong tiêu chuẩn này sử dụng các kí hiệu sau:
c nồng độ chất;
ρ nồng độ khối lượng;
g gia tốc trọng trường trên bề mặt trái đất (9,81 m/s2).
3.2. Chữ viết tắt
Trong tiêu chuẩn này sử dụng các chữ viết tắt sau:
ACS Axetyl coenzym A synthetaza;
CoA Coenzym A;
ATP Adenosin-5'-tri-phosphat; AMP Adenosin-mono-phosphat;
CS Xitrat synthaza;
NAD β-Nicotinamit-adenin-dinucleotit;
NADH β-Nicotinamit-adenin-dinucleotit, dạng khử;
MDH Malat-dehydrogenaza;
IU 1 đơn vị quốc tế (IU) hoạt độ enzym xúc tác chuyển đổi được 1 µmol cơ chất mỗi phút ở 25 oC trong điều kiện chuẩn.
4. Nguyên tắc
Axit axetic (axetat) được chuyển hóa thành axetyl-CoA (phản ứng 1) khi có mặt enzym axetyl-coenzym A-synthetaza (ACS) cùng với adenosin-5'-tri-phosphat (ATP) và coenzym A (CoA):
Axetat + ATP + CoA ![]() axetyl-CoA
+ AMP + pyrophosphat (1)
axetyl-CoA
+ AMP + pyrophosphat (1)
Axetyl-CoA phản ứng với oxaloaxetat sinh ra xitrat, khi có mặt xitrat synthaza (CS) (phản ứng 2):
Axetyl-CoA + oxaloaxetat + H2O ![]() xitrat + CoA (2)
xitrat + CoA (2)
Oxaloaxetat cần cho phản ứng (2) được tạo thành từ malat và nicotinamit-adenin dinucleotit (NAD) khi có mặt malat dehydrogenaza (MDH) (phản ứng 3). Trong phản ứng này, NAD được khử thành NADH.
Malat + NAD+ ![]() oxaloaxetat
+ NADH + H+ (3)
oxaloaxetat
+ NADH + H+ (3)
Phép xác định dựa trên sự tạo thành NADH, được đo bằng sự độ tăng độ hấp thụ ở bước sóng 340 nm, 334 nm hoặc 365 nm. Do sử dụng phản ứng chỉ thị trước, lượng NADH tạo thành tỉ lệ với nồng độ axit axetic nhưng không phải là hàm tuyến tính.
5. Thuốc thử
5.1. Yêu cầu chung
Chỉ sử dụng thuốc thử tinh khiết phân tích và nước loại 3 nêu trong TCVN 4851:1989 (ISO 3696:1987).
CHÚ THÍCH: Phép xác định có thể được thực hiện bằng cách sử dụng bộ kit thử phức hợp có bán sẵn trên thị trường.
5.2. Trietanolamin hydroclorua.
5.3. Axit L-malic.
5.4. Magie clorua, MgCl2.6H2O.
5.5. Dung dịch kali hydroxit, c(KOH) = 2 mol/l.
5.6. Nicotinamit-adenin dinucleotit (khoảng 98 %).
5.7. Coenzym A.
5.8. Muối dinatri của adenosin-5'-triphosphat, ATP-Na2H2.
5.9. Natri hydrocacbonat, NaHCO3.
5.10. Malat dehydrogenaza, huyền phù trong amoni sulfat, c(MDH) = 3,2 mol/l, hoạt độ riêng khoảng 1 200 IU/mg.
5.11. Xitrat synthaza, huyền phù trong amoni sulfat, c(CS) = 3,2 mol/l, hoạt độ riêng khoảng 110 IU/mg.
5.12. Axetyl-CoA synthetaza, dạng đông khô.
5.13. Amoni sulfat, (NH4)2SO4.
5.14. Natri axetat, CH3COONa.3H2O.
5.15. Dung dịch đệm, pH = 8,4
Hoà tan 7,59 g trietanolamin hydroclorua (5.2), 420 mg axit malic (5.3) và 210 mg magie clorua (5.4) trong khoảng 70 ml nước. Chỉnh pH của dung dịch tới ph 8,4 với khoảng 21 ml dung dịch kali hydroxit (5.5) và thêm nước đến 100 ml. Dung dịch đệm đã pha bền được 4 tuần ở + 4 oC.
5.16. Dung dịch nicotinamit-adenin dinucleotit/Coenzym A
Hòa tan 144 mg NAD (5.6) và 30 mg CoA (5.7) trong 6 ml nước. Dung dịch đã pha bền được 1 tuần ở + 4 oC.
5.17. Dung dịch adenosin-5'-triphosphat
Hoà tan 300 mg ATP-Na2H2 (5.8) và 300 mg natri hydrocacbonat (5.9) trong 6 ml nước. Dung dịch đã pha bền được 4 tuần ở + 4 oC.
5.18. Huyền phù malat dehydrogenaza/xitrat synthaza
Trộn 0,6 ml huyền phù MDH (5.10) và 0,6 ml huyền phù CS (5.11). Huyền phù đã pha bền được 1 năm ở + 4 oC.
5.19. Huyền phù axetyl-CoA synthetaza
Hoà tan 20 mg ACS dạng đông khô (5.12) trong 0,5 ml dung dịch amoni sulfat (5.20). Huyền phù đã pha bền được 2 tuần ở + 4 oC.
5.20. Dung dịch amoni sulfat, c((NH4)2SO4) = 1 mol/l
Hoà tan 13,2 g amoni sulfat (5.13) trong khoảng 80 ml nước, chỉnh đến pH 7,3 bằng khoảng 0,2 ml dung dịch kali hydroxit (5.5) và thêm nước đến 100 ml. Dung dịch đã pha bền được 1 năm ở 20 oC đến 25 oC.
5.21. Dung dịch chuẩn axetat, c(CH3COO–) = 5 mmol/l
Hòa tan 68 mg natri axetat (5.14) trong 100 ml nước. Chuẩn bị dung dịch mới trước khi sử dụng.
6. Thiết bị, dụng cụ
Sử dụng thiết bị, dụng cụ của phòng thử nghiệm thông thường và cụ thể như sau:
6.1. Pipet dùng để thử nghiệm enzym, có chia vạch dọc thân pipet và đầu tip phân phối dài, không chia vạch.
6.2. Pipet, có độ chính xác tương đương 6.1 (thay thế cho 6.1), ví dụ có thể thay đổi dung tích của pipet.
6.3. Cuvet, làm bằng thạch anh, thủy tinh hoặc bằng nhựa, có chiều dài đường quang 1 cm và có độ hấp thụ không đáng kể ở các bước sóng 334 nm, 340 nm và 365 nm.
6.4. Máy đo quang đơn phổ, có đèn thủy ngân và màng lọc đo được ở các bước sóng 334 nm hoặc 365 nm.
6.5. Máy đo quang phổ, (bước sóng có thể thay đổi) để đo ở 340 nm (thay thế cho 6.4).
6.6. Máy li tâm, có thể tạo gia tốc li tâm 3000g trên các ống li tâm (6.8).
CHÚ THÍCH: Tần số quay cần thiết để tạo gia tốc li tâm chính xác có thể được tính từ công thức sau:
a = 11,18 x r x (n/1 0002) (4)
trong đó:
a là gia tốc li tâm;
r là bán kính của máy li tâm, tính bằng centimet (cm), được đo từ trung điểm (trên trục li tâm) đến đáy của ống li tâm khi quay;
n là số vòng quay trong một phút.
6.7. Thiết bị lọc màng, với màng lọc có cỡ lỗ 0,45 µm.
6.8. Ống li tâm.
7. Cách tiến hành
7.1. Chuẩn bị mẫu thử
Pha loãng nước quả sao cho hàm lượng axit axetic trong mỗi cuvet có khoảng từ 1 µg đến 30 µg. Hàm lượng này tương đương với 10 mg đến 300 mg axit axetic trong một lít mẫu thử (dạng dung dịch). Nếu nồng độ axit axetic trong mẫu thử (dạng dung dịch) nhỏ hơn 10 mg/l, thể tích mẫu được cho vào cuvet có thể tăng đến 1,5 ml. Trong trường hợp này, thể tích nước được thêm vào phải giảm đi sao cho thể tích cuối cùng trong cuvet là không đổi.
Sử dụng ngay mẫu (đã pha loãng), kể cả khi mẫu có màu nhạt.
Việc phân tích theo phương pháp này phải thực hiện dựa vào đơn vị thể tích, kết quả được biểu thị theo lít mẫu thử. Việc phân tích các mẫu cô đặc có thể được thực hiện dựa theo thể tích sau khi pha loãng đến tỉ trọng tương đối đã biết. Trong trường hợp này, phải đưa ra được tỉ trọng tương đối. Dựa trên lượng mẫu đã cân và đưa hệ số pha loãng khi phân tích vào phép tính, kết quả có thể được biểu thị theo kilogam sản phẩm. Đối với các sản phẩm có độ nhớt cao và/hoặc có hàm lượng tế bào rất cao (ví dụ thịt quả), việc xác định dựa trên lượng mẫu thử đã cân theo quy trình thông thường.
Đối với mẫu đục thì trộn kĩ trước khi pha loãng. Làm trong các mẫu dạng đục có nồng độ axit axetic thấp bằng cách lọc qua màng lọc 0,45 µm (6.7) và li tâm.
7.2. Tiến hành thử
7.2.1. Yêu cầu chung
Phép xác định phải thực hiện trong điều kiện nhiệt độ không đổi, trong khoảng từ 20 oC đến 25 oC. Có thể sử dụng nhiệt độ không đổi trong khoảng từ 25 oC đến 37 oC, với điều kiện thu được các kết quả tương đương.
NADH có độ hấp thụ cực đại tại bước sóng 340 nm. Khi sử dụng máy đo phổ thay đổi được bước sóng (6.5), thì chỉ đo tại bước sóng hấp thụ cực đại. Khi sử dụng máy đo quang phổ đơn dùng đèn hóa hơi thủy ngân, thì đo tại bước sóng 334 nm hoặc 365 nm.
Không sử dụng pipet một vạch để hút dung dịch. Các dung dịch enzym, coenzym và đệm có thể được lấy bằng pipet tự động thích hợp. Chỉ sử dụng pipet dùng để thử nghiệm enzym (6.1) hoặc dụng cụ tương đương (6.2) để lấy dung dịch mẫu thử. Sử dụng dung dịch chuẩn axit axetic trong mỗi dãy phân tích.
7.2.2. Dung dịch mẫu trắng
Xem thêm về quy trình lấy dung dịch mẫu thử bằng pipet tại 7.2.3.
Dùng pipet lấy 1,00 ml dung dịch đệm (5.15), 0,10 ml dung dịch NAD/CoA (5.16), 0,10 ml dung dịch ATP (5.17) và 2,00 ml nước cho vào cuvet.
Trộn và đọc độ hấp thụ A0 sau 3 min.
Thêm 0,02 ml dung dịch MDH/CS (5.18), trộn và đọc độ hấp thụ A1 sau 2 min.
Thêm 0,01 ml huyền phù ACS (5.19), trộn và đọc độ hấp thụ A2 sau 10 min đến 15 min.
7.2.3. Dung dịch thử axit axetic
Dùng pipet lấy 1,00 ml dung dịch đệm (5.15), 0,10 ml dung dịch NAD/CoA (5.16), 0,10 ml dung dịch ATP (5.17), 0,10 ml dung dịch mẫu thử (7.1) và 1,90 ml nước cho vào cuvet.
Trộn và đọc độ hấp thụ A0 sau 3 min.
Thêm 0,02 ml dung dịch MDH/CS (5.18), trộn và đọc độ hấp thụ A1 sau 2 min.
Thêm 0,01 ml huyền phù ACS (5.19), trộn và đọc độ hấp thụ A2 sau khi phản ứng kết thúc (khoảng 10 min đến 15 min).
Kiểm tra phản ứng đã kết thúc hay chưa bằng cách cứ sau 2 min trong khoảng thời gian 10 min, đọc các độ hấp thụ cuối cùng. Nếu cần, điều chỉnh phản ứng "phụ" (giá trị tăng lên không đổi) bằng cách ngoại suy độ hấp thụ về thời điểm thêm MDH/CS (xem Phụ lục B).
Bảng 1
|
Dùng pipet cho vào cuvet |
Mẫu trắng, ml |
Mẫu thử, ml |
|
Dung dịch đệm (5.15) Dung dịch NAD/CoA (5.16) Dung dịch ATP (5.17) Dung dịch mẫu thử (7.1) Nước |
1,00 0,10 0,10 – 2,00 |
1,00 0,10 0,10 0,10 1,90 |
|
Trộn và đọc độ hấp thụ A0 của dung dịch sau khoảng 3 min, sau đó thêm: |
||
|
Dung dịch MDH/CS (5.18) |
0,02 |
0,02 |
|
Trộn và đọc độ hấp thụ A1 của dung dịch sau khoảng 2 min. Bắt đầu phản ứng bằng cách thêm: |
||
|
Huyền phù ACS (5.19) |
0,01 |
0,01 |
|
Trộn và sau khi phản ứng kết thúc (khoảng 15 min), đọc độ hấp thụ A2 của mẫu trắng và mẫu thử. Nếu phản ứng chưa kết thúc sau 15 min, cứ sau 2 min tiếp tục đọc độ hấp thụ, cho đến khi độ hấp thụ tăng đều trong 10 min. |
||
Chỉnh phản ứng "phụ" có thể xảy ra bằng cách ngoại suy độ hấp thụ về thời điểm thêm ACS (xem Phụ lục B).
Xác định chênh lệch độ hấp thụ đối với mẫu trắng và mẫu thử (A1 – A0) và (A2 – A0).
Với các phản ứng chỉ thị trước, không có mối quan hệ tuyến tính giữa chênh lệch độ hấp thụ đo được và nồng độ axit axetic.
Công thức sau dùng để tính ΔAaxit axetic:
![]()
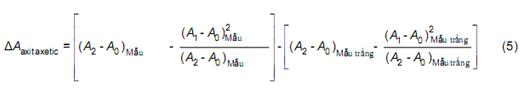
8. Tính kết quả
Hàm lượng axit axetic, ρ, biểu thị bằng miligam trên lít (mg/l) được tính theo công thức sau:
![]() (6)
(6)
Trong đó:
V1 là thể tích cuối cùng, tính bằng mililit (ml);
M là khối lượng phân tử của axit axetic (60,05 g/mol);
F là hệ số pha loãng dung dịch mẫu thử;
V2 là thể tích của dung dịch mẫu thử, tính bằng mililit (ml);
d là chiều dài đường quang của cuvet, tính bằng centimet (cm);
ε là hệ số hấp thụ của NADH
tại bước sóng 340 nm, ε = 6,3 [l × mmol– 1 × cm– 1];
tại bước sóng 365 nm, ε = 3,4 [l × mmol– 1 × cm– 1];
tại bước sóng 334 nm, ε = 6,18 [l × mmol– 1 × cm– 1].
Nếu không thay đổi các thể tích trong 7.2.2 và 7.2.3, thì tính hàm lượng axit axetic bằng miligam trên lít (mg/l) của mẫu theo công thức sau:
![]() (7)
(7)
Khi sử dụng bộ kit thử phức hợp có bán sẵn trên thị trường, thì hệ số 1 940 trong công thức (7) nêu trên có thể thay đổi.
Trong phần tính kết quả, cần tính đến hệ số pha loãng và mối tương quan giữa giá trị với thể tích hoặc khối lượng. Nếu sản phẩm cô đặc đã được pha loãng đến nồng độ đơn thì ghi lại tỉ trọng tương đối của mẫu nồng độ đơn.
Tính hàm lượng axit axetic theo miligam trên lít đến số nguyên hoặc theo miligam trên kilogam, phụ thuộc vào việc chuẩn bị mẫu (7.1).
9. Độ chụm
Chi tiết về phép thử liên phòng thử nghiệm về độ chụm của phương pháp được đưa ra trong Phụ lục A. Các giá trị thu được từ phép thử liên phòng này có thể không áp dụng được cho các dải nồng độ và chất nền khác với dải nồng độ và chất nền nêu trong Phụ lục A.
9.1. Độ lặp lại
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ thu được khi sử dụng cùng phương pháp, tiến hành trên vật liệu thử giống hệt nhau, do một người thực hiện, sử dụng cùng thiết bị, trong một khoảng thời gian ngắn, không được quá 5 % các trường hợp vượt quá giá trị độ lặp lại r.
Giá trị độ lặp lại:
r = 19 mg/l.
9.2. Độ tái lập
Chênh lệch tuyệt đối giữa hai kết quả thử riêng rẽ thu được khi sử dụng cùng phương pháp, tiến hành thử trên vật liệu giống thử hệt nhau, trong các phòng thử nghiệm khác nhau, do những người khác nhau thực hiện, sử dụng các thiết bị khác nhau, không được quá 5 % các trường hợp vượt quá giá trị độ tái lập R.
Giá trị độ tái lập:
R = 49 mg/l.
10. Báo cáo thử nghiệm
Báo cáo thử nghiệm phải ghi rõ:
– mọi thông tin cần thiết để nhận biết đầy đủ về mẫu thử (loại mẫu, nguồn gốc của mẫu, tên gọi);
– viện dẫn tiêu chuẩn này;
– ngày và phương pháp lấy mẫu, nếu biết;
– ngày nhận mẫu;
– ngày thử nghiệm;
– kết quả thử và đơn vị biểu thị kết quả;
– độ lặp lại, nếu được kiểm tra;
– bất kỳ điểm ngoại lệ nào quan sát được trong khi thực hiện phép thử;
– mọi thao tác không quy định trong phương pháp hoặc tùy chọn mà có thể ảnh hưởng đến kết quả.
PHỤ LỤC A
(Tham khảo)
Kết quả thống kê phép thử liên phòng thử nghiệm
Theo ISO 5725:1986*, các thông số sau đây đã được xác định trong một phép thử liên phòng thử nghiệm (Thư mục tài liệu tham khảo). Phép thử được tiến hành bởi Intermational Federal of Fruit Juice Producers (IFU), Paris, Pháp.
|
Năm tiến hành thử nghiệm: Số lượng phòng thử nghiệm tham gia: Số lượng mẫu thử: |
1991/1 22 2 |
1991/2 21 2 |
![]() Bảng A.1
Bảng A.1
|
Mẫu |
A |
B |
C |
D |
|
Số lượng phòng thử nghiệm còn lại sau khi trừ ngoại lệ Số lượng ngoại lệ (phòng thử nghiệm) Số lượng kết quả được chấp nhận |
19 3 77 |
16 6 65 |
21 – 83 |
20 1 80 |
|
Giá trị trung bình ( |
252 |
325 |
249 |
215 |
|
Độ lệch chuẩn lặp lại (sr) (mg/l) Độ lệch chuẩn tương đối lặp lại (RSDr) (%) |
7,65 3,0 |
8,28 2,6 |
5,30 2,1 |
5,11 2,4 |
|
Giới hạn lặp lại (r) (mg/l) |
22 |
23 |
15 |
14 |
|
Độ lệch chuẩn tái lập (sR) (mg/l) Độ lệch chuẩn tương đối tái lập (RSDR) (%) |
18,69 7,4 |
23,62 7,3 |
11,69 4,7 |
15,55 7,2 |
|
Giới hạn tái lập (R) (mg/l) |
53 |
66 |
33 |
44 |
Tên mẫu:
A – nước cà chua,
B – nectar anh đào,
C – nước táo,
D – nước cam.
PHỤ LỤC B
(Tham khảo)
Thông tin về cách xử lí các phản ứng "phụ"
Các phản ứng "phụ" nói chung do tác dụng phụ của enzym, sự có mặt của các enzym khác trong chất nền mẫu thử, hoặc do tương tác của một hoặc một số thành phần của chất nền với thuốc thử của phản ứng enzym.
Trong phản ứng thông thường, độ hấp thụ thu được là giá trị không đổi sau khoảng thời gian xác định, thông thường từ 10 min đến 20 min, phụ thuộc vào tốc độ của phản ứng enzym cụ thể. Tuy nhiên, khi phản ứng xảy ra, mà độ hấp thụ không đạt được giá trị không đổi mà tăng đều theo thời gian và dạng phản ứng này được gọi chung là phản ứng "phụ".
Nếu có phản ứng "phụ" xuất hiện, thì độ hấp thụ của dung dịch phải được đo trong các khoảng thời gian cách đều (2 min đến 5 min) sau thời gian cần thiết để dung dịch đạt độ hấp thụ cuối cùng. Khi độ hấp thụ tăng theo tỉ lệ không đổi (dA/dt = hằng số), đọc từ 5 lần đến 6 lần và sau đó ngoại suy, dùng biểu đồ hoặc dùng phép tính, để thu được độ hấp thụ của dung dịch tại thời điểm cuối cùng khi enzym được thêm vào (To). Chênh lệch của độ hấp thụ ngoại suy tại thời điểm này (Af – Ai) được sử dụng để tính nồng độ chất nền.
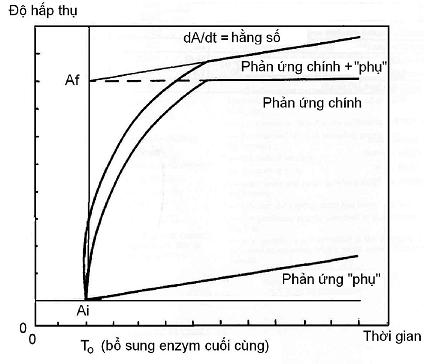
Hình B.1 – Phản ứng phụ
THƯ MỤC TÀI LIỆU THAM KHẢO
[1] ISO 5725:1986 Precision of test methods – Determination of repeatability and reproducibility for a standard test method by inter-laboratory tests (Độ chụm của phương pháp thử – Xác định độ lặp lại và độ tái lập của phương pháp thử bằng thử nghiệm liên phòng).
[2] Determination of acetic acid: Enzymatic method, No. 66,1996, Analyses [Collection] International Federation of Fruit Juice Producers. Loose-leaf edition, as of 1996. Zug: Swiss Fruit Union.
[3] Determination of acetic acid: Enzymatic method, Methods of biochemical analysis and food analysis using single reagents. Boehringer Mannheim.
* ISO 5725:1986 hiện nay đã hủy, được thay bằng ISO 5725 (gồm có 6 phần) và đã được biên soạn thành bộ TCVN 6910 (gồm có 6 phần).
