Tiêu chuẩn Việt Nam TCVN 6427-1:1998 (ISO 6557/1 : 1986) về rau, quả và các sản phẩm rau quả - xác định hàm lượng axit ascorbic - phần 1: phương pháp chuẩn do Bộ Khoa học Công nghệ và Môi trường
TIÊU CHUẨN VIỆT NAM
TCVN 6427-1 : 1998
RAU,
QUẢ VÀ CÁC SẢN PHẨM RAU QUẢ - XÁC ĐỊNH HÀM LƯỢNG AXIT ASCORBIC - PHẦN 1: PHƯƠNG
PHÁP CHUẨN
Fruit, vegetables and derived products – Determination of ascorbic acid - Part
1: Reference methods
Lời nói đầu
TCVN 6427-1 : 1998 hoàn toàn tương đương với ISO 6557/1 : 1986
TCVN 6427-1 : 1998 do Ban kỹ thuật Tiêu chuẩn TCVN/TC/F10 Rau quả và sản phẩm rau quả biên soạn, Tổng cục Tiêu chuẩn – Đo lường – Chất lượng đề nghị và được Bộ Khoa học Công nghệ và Môi trường ban hành.
1. Phạm vi và lĩnh vực áp dụng
Tiêu chuẩn này quy định phương pháp chuẩn để xác định hàm lượng axit ascorbic và dehidroascorbic được kết hợp trong rau quả và sản phẩm rau quả, bằng cách dùng phổ kế huỳnh quang phân tử.
2. Nguyên tắc
Chuyển đổi axit ascorbic thành axit dehidroascorbic bằng than hoạt tính.
Phản ứng của axit dehidroascorbic với o-phenylendiamin (OPDA) cho hợp chất huỳnh quang theo phản ứng sau đây:
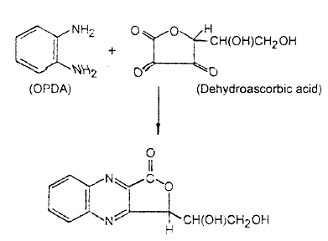
(-Oxo-2 4 H-3-(1,2-dihidroxyetyl) furo[3,4-b] quinoxalin)
Khi kiểm tra sự có mặt của axit boric, việc tạo thành phức chất H3BO3 – axit dehidroascorbic ngăn cản phản ứng với OPDA. Do vậy, bất kỳ ảnh hưởng huỳnh quang nào cũng phải được tính đến trong khi tính kết quả.
Chú thích – Hàm lượng axit dehidroascorbic đơn lẻ ban đầu có thể được xác định bỏ qua bước sử dụng than hoạt tính. Sau đó có thể bằng phép trừ đi để tính hàm lượng axit ascorbic đơn lẻ ban đầu.
3. Thuốc thử và vật liệu
Sử dụng tất cả các thuốc thử loại phân tích và sử dụng nước cất hoặc nước có độ tinh khiết tương đương.
3.1 Dung dịch O-Phenylendiamin dihidroclorua (C6H8N2.2HCl), 0,2g/l.
Chuẩn bị dung dịch này ngay trước khi sử dụng.
3.2 Dung dịch natri axetat ngậm ba phân tử nước (CH3COONa.3H2O), 500g/l.
3.3 Dung dịch axit boric/natri axetat.
Hòa tan 3g axit boric (H3BO3) trong 100ml dung dịch natri axetat (3.2)
Chuẩn bị dung dịch này ngay trước khi sử dụng.
3.4 Axit ascorbic, dung dịch chuẩn 1 g/l.
Cân 50mg axit ascorbic chính xác đến 0,01mg, trước đó đã khử nước trong bình hút ẩm tránh ánh sáng. Chuyển sang bình định mức dung tích 50ml và thêm dung dịch chiết cho đến vạch (3.5) trước khi sử dụng.
3.5 Dung dịch chiết
3.5.1 Axit metaphotphoric/axit axetic
Cho 30g axit metaphotphoric (HPO3) vào cốc hoặc sang bình nón dung tích 1 000ml có chứa 80ml axit axetic bằng (CH3COOH) và khoảng 500ml nước. Đun nóng và khuấy nhẹ cho đến khi tan hết.
Để dung dịch nguội. Chuyển toàn bộ sang bình đựng mức dung tích 1000ml và thêm nước cho đến vạch.
Hoặc
3.5.2 Axit metaphotphoric/metanola
Trộn ba thể tích dung dịch axit metaphotphoric 4% (m/m) với 1 thể tích metanola.
Chú thích – Axit metaphotphoric có bán sẵn với hàm lượng HPO3 từ 40% đến 44%
3.6 Than hoạt tính
Cân 200g than hoạt tính và thêm vào 1l axit clohidric 10% (v/v).
Đun đến sôi, sau đó lọc qua bộ lọc thủy tinh xốp có độ xốp p 40 (từ 16μm đến 40μm ). Cho “bánh” cacbon vào cốc có mỏ. Thêm 1 lít nước, lắc và lọc kỹ qua bộ lọc thủy tinh xốp. Lặp lại 3 lần thao tác rửa với nước và lọc.
Cho phần cặn vào tủ sấy đặt ở nhiệt độ 1150C±50C và để 12h (thí dụ như để qua đêm).
4. Thiết bị
Sử dụng thiết bị thí nghiệm thông thường và thiết bị đặc biệt như:
4.1 Máy nghiền cơ học.
4.2 Máy li tâm.
4.3 Que khuấy, để dùng với bình nón và ống nghiệm.
4.4 Phổ kế huỳnh quang phân tử. Bước sóng kích thích và phát xạ tối ưu cho mẫu phân tích phải được xác định trước và phụ thuộc vào dụng cụ sử dụng. Nó được gắn với đèn phát quang phổ liên tục.
4.5 Bình nón có dung tích thích hợp.
4.6 Bình định mức, dung tích 100ml.
4.7 Ống nghiệm, có đường kính 10mm.
4.8 Pipet, có dung tích thích hợp.
4.9 Giấy lọc.
5. Cách tiến hành
5.1 Chuẩn bị mẫu thử
Nghiền trộn kỹ mẫu thí nghiệm. Nếu cần, trước tiên loại bỏ các hạt và các vách cứng của khoang chứa hạt và cho mẫu thí nghiệm vào máy nghiền cơ học (4.1). Để cho sản phẩm đông lạnh tan giá trong bình đậy kín và đồng thời đổ chất lỏng đã tan vào mẫu thí nghiệm trước khi nghiền trộn.
5.2 Phần mẫu thử
Lấy một lượng mẫu thử (5.1), cân chính xác đến 0,1mg, cho vào bình nón (4.5) sao cho sau khi pha loãng bằng dung dịch chiết, hàm lượng axit ascorbic và axit dehidroascorbic dự kiến trong khoảng 0-50mg/l.
5.3 Chuẩn bị dung dịch thử
5.3.1 Cho một lượng xác định dung dịch chiết (3.5) vào phần mẫu thử sao cho hàm lượng axit ascorbic và axit dehidroascorbic dự kiến trong khoảng 0-50mg/l. Khuấy trong 30 phút và chạy ly tâm. Chỉnh pH đến 1,2 bằng một thể tích dung dịch chiết (3.5) đã đong.
Lấy 100ml dung dịch này và cho thêm 1 g than hoạt tính (3.6). Trộn kỹ, sau đó lọc qua giấy lọc (4.9), loại bỏ vài mililit dịch lọc đầu tiên.
5.3.2 Dùng pipet (4.8), lấy 5ml dung dịch natri axetat (3.2) và 5ml dịch lọc (5.3.1) cho vào định mức dung tích 100ml (4.6). Trộn và thêm nước cho đến vạch.
5.4 Thử đối chiếu
Dùng pipet lấy 5ml dung dịch axit boric/natri axetat (3.3) và 5 ml dịch lọc (5.3.1) cho vào bình định mức dung tích 100 ml. Để 15 phút, thỉnh thoảng lắc trộn sau đó thêm nước cho đến vạch.
5.5 Xác định
Cho 2 ml dung dịch thử (5.3.2) vào ống nghiệm (4.7) và cho 2 ml dung dịch thử đối chiếu (5.4) vào ống nghiệm khác.
Thêm 5 ml dung dịch O-Phenylendiamin dihidroclorua (3.1) vào mỗi ống nghiệm, tránh ánh sáng chiếu vào. Dùng khe khuấy (4.3) khuấy kỹ, sau đó để trong bóng tối 30 phút cho phản ứng xảy ra.
Tiến hành đo cả hai ống bằng phổ kế huỳnh quang phân tử (4.4) đã được hiệu chỉnh trước, dùng đèn công suất tối thiểu. Lấy số đọc được của dung dịch thử trừ đi số đọc của dung dịch thử đối chiếu.
5.6 Đồ thị chuẩn
5.6.1 Dùng pipet lấy 2ml và 5ml dung dịch chuẩn (3.4) cho vào hai bình định mức dung tích 100ml. Cho dung dịch chiết đến vạch (3.5). Hai dung dịch này chứa 20mg và 50mg axit ascorbic trong 1 lít.
Thêm vào mỗi dung dịch này 1 g than hoạt tính (3.6). Khuấy trộn kỹ, sau đó lọc qua giấy lọc (4.9), loại bỏ vài mililit dịch lọc đầu tiên.
5.6.2 Lặp lại các thao tác 5.3.2, 5.4, và 5.5 với cả hai dung dịch hiệu chuẩn (5.6.1), thay 5 ml dịch lọc bằng 5 ml của mỗi dung dịch hiệu chuẩn.
Dựng đồ thị chuẩn theo số đo quang phổ và nồng độ của cả hai dung dịch hiệu chuẩn và tính bằng miligam trên lít.
Vẽ đồ thị chuẩn đi qua gốc tọa độ và hai điểm thu được.
5.7 Số lần xác định
Tiến hành hai lần xác định trên cùng mẫu thử (5.1)
6. Biểu thị kết quả
Hàm lượng axit ascorbic và axit dehidroascorbic, biểu thị bằng miligam trên 100g sản phẩm, được tính theo công thức sau:
![]()
trong đó
m0 là khối lượng của phần mẫu thử, tính bằng gam;
V là thể tích của dung dịch chiết thêm vào, tính bằng mililit;
c là nồng độ của axit ascorbic và axit dehidroascorbic có trong phần mẫu thử đọc từ đồ thị chuẩn và được hiệu chỉnh theo dung dịch thử đối chiếu, tính bằng miligam trên lít.
7. Báo cáo kết quả
Báo cáo kết quả phải chỉ ra phương pháp đã sử dụng và kết quả thử nghiệm thu được. Cũng phải đề cập đến tất cả các chi tiết thao tác không qui định trong tiêu chuẩn này, cùng với các chi tiết bất thường nào khác có thể ảnh hưởng tới kết quả.
Báo cáo kết quả cũng bao gồm tất cả các thông tin cần thiết về việc nhận biết đầy đủ về mẫu thử.
